La
adrenalina o epinefrina, es una hormona y un neurotransmisor secretado por las
glándulas suprarrenales (que están sobre los riñones) cuando hay situaciones de
alerta, de peligro y miedo. Sirve para que el organismo se prepare ante
situaciones de emergencia. También existe la adrenalina sintética que se
utiliza como medicamento (inyectable) para tratar reacciones asmáticas o
alérgicas potencialmente mortales. El término adrenalina deriva de las raíces latinas ad- y renes que
literalmente significan “junto al riñón”, en referencia a su ubicación
anatómica. El término epinefrina tiene
un significado similar, deriva de las raíces griegas epi- y nephron que
significan “sobre el riñón”.
En
1886 William Bates anunció el descubrimiento de una sustancia producida por las
glándulas suprarrenales. El químico japonés Jokichi Takamine la aisló y
purificó (en 1901) de las glándulas suprarrenales de ovejas y bueyes. Fue la
primera hormona que se pudo cristalizar y el primer broncodilatador eficaz para
el asma. Su estructura fue determinada por Jowett y fue sintetizada en 1904,
independientemente, por Friedrich Stolz y Henry Drysdale Dakin.
La
adrenalina se produce en la médula de las glándulas suprarrenales a partir de
los aminoácidos fenilalanina y tirosina a través de una serie de productos
intermedios. Es almacenada y, ante situaciones de riesgo, es liberada. Actúa
sobre casi todos los tejidos del cuerpo principalmente los músculos, el tejido
adiposo y el hígado: relaja la musculatura de las vías respiratorias y aumenta
la velocidad de respiración (ingresa más aire a los pulmones), estimula el
corazón (latidos con mayor fuerza y rapidez), retarda la digestión y aumenta la
glucosa en sangre (más sangre y energía para los músculos), dilata las pupilas
(mayor capacidad de observación), contrae los vasos sanguíneos, aumenta la
presión, etc. Todos estos efectos preparan al cuerpo para una mejor reacción
ante los peligros, dejándolo listo para la lucha o la huida.
El
plasma de un adulto en reposo contiene adrenalina en una concentración menor a
los 10 ng/L (nanogramos por litro), durante el ejercicio puede subir unas 10
veces y, durante el estrés, llegar a unas 50 veces este valor. Los principales
desencadenantes fisiológicos de la liberación de adrenalina son las tensiones
tales como las amenazas físicas, las emociones intensas, los ruidos, las luces
brillantes y la alta temperatura ambiental. Comienza a liberarse en cuestión de
segundos, alcanza su punto más alto al minuto y su efectividad se extiende entre
uno y tres minutos, tiene la capacidad de aumentar el metabolismo normal del
cuerpo hasta en un 100%.
Su
molécula es relativamente pequeña (C9H13NO3), es
muy soluble en agua, forma cristales blancos y es sensible a la luz y al aire, se
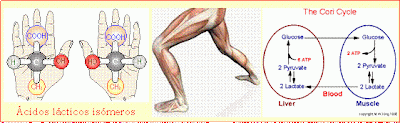
descompone dando productos oscuros. La molécula tiene un átomo de carbono
asimétrico o quiral, por lo que existen dos formas (isómeros ópticos) en los
que uno es la imagen en el espejo del otro (enantiómeros). El isómero natural y
el que posee actividad farmacológica es la forma levógira o R(-)adrenalina. El
isómero dextrógiro o S(+)adrenalina carece de actividad farmacológica. Con fines médicos se usa la adrenalina sintética que
contiene ambos isómeros en proporción 1:1 (es una mezcla racémica o racemato).
La
adrenalina no se puede administrar por vía oral porque se descompone en el
aparato digestivo. Se aplica por vía sub-lingual, o mediante inyecciones
sub-cutáneas (debajo de la piel) o mejor aún por vía intramuscular (más
profunda que la sub-cutánea) que es de acción más rápida. También pueden usarse
otras vías (intravenosa, nebulización, intratraqueal o incluso intracardíaca)
pero éstas sólo se aplican dentro de hospitales. Su uso puede ser riesgoso si
no se toman las precauciones adecuadas.
La
adrenalina se usa para el tratamiento de reacciones alérgicas graves. Las
reacciones alérgicas pueden ser de tipo asma, rinitis, conjuntivitis, de piel, inflamación,
digestivas o generalizadas como la anafilaxia. La gravedad de ellas varía mucho
de un paciente a otro. Cuando la reacción es una amenaza para la vida, el tratamiento
de urgencia es la adrenalina. Así, en casos agudos de asma, que casi no
permiten la respiración, una inyección de adrenalina dilata los bronquios y
reduce la inflamación en forma casi instantánea. También se usa en casos de
reacciones alérgicas agudas y graves (como alergias por alimentos,
medicamentos, picaduras de insectos, etc.). Sus efectos son muy rápidos, casi
instantáneos y de corta duración, por lo que a veces hay que repetir la aplicación
cada 15 a
20 minutos.
BIBLIOGRAFÍA
http://www.seicap.es/adrenalina.asp
Q.F. JUAN JOSÉ LEÓN CAM <jjleon@lamolina.edu.pe>
Departamento de Química. Universidad Nacional Agraria La Molina. PERÚ.