La bolsa de aire, en inglés “airbag”, es un sistema de seguridad pasiva que se instala en los automóviles para proteger a sus ocupantes en casos de choque, actuando como una barrera que evita los golpes violentos contra la superficie rígida del interior del vehículo. Se basa en una idea sencilla: al producirse el choque, la bolsa de plástico se infla inmediatamente con un gas (que no es aire) y las personas son amortiguadas por esta bolsa llena de gas. A pesar de lo simple que parezca la idea, su desarrollo necesitó de los esfuerzos de químicos e ingenieros.
El sistema requiere de una bolsa con características especiales: 1) no debe inflarse accidentalmente, pues obstaculizaría la visión del conductor; 2) el gas utilizado no debe ser tóxico, pues al escaparse produciría daños por inhalación; 3) el gas deberá obtenerse muy rápidamente para que la bolsa esté llena antes que las personas impacten sobre ella y, finalmente, 4) los productos químicos generadores del gas deben ser de fácil manejo y estables durante largos periodos de tiempo.
Luego de la evaluación de varios gases no tóxicos, se decidió que el nitrógeno (N2) era el más adecuado, pues constituye cerca del 79% en volumen del aire. Una buena manera de obtenerlo es por descomposición de la azida de sodio, según la siguiente ecuación:
2 NaN3(s) ® 2 Na(s) + 3 N2(g)
azida de sodio sodio nitrógeno
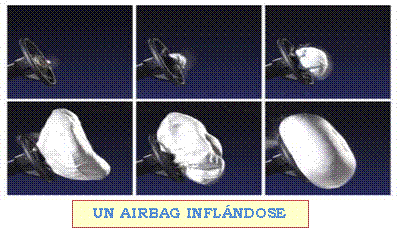
Se ha calculado que, en condiciones ambientales, 130 gramos de azida de sodio producen cerca de 60 litros de gas nitrógeno, cantidad suficiente para inflar la bolsa protectora. Al producirse el impacto, un sensor genera una chispa eléctrica y ésta provoca la explosión de la azida, generando el nitrógeno que infla la bolsa. La reacción química es de alta velocidad y el airbag tarda 58 milésimas de segundo en inflarse desde que la pastilla (conteniendo la azida de sodio) recibe el impulso eléctrico. Este mecanismo se torna peligroso si no se lleva cinturón de seguridad, ya que está calculado para recibir el impacto del pasajero después que los pretensores hayan tensado el cinturón sobre el tórax y, si esta frenada no se produce, la cabeza puede abalanzarse hacia delante sin tiempo suficiente para que la bolsa se llene.
En 1980 los problemas de diseño estaban resueltos, pero no así los problemas de naturaleza química. Las pastillas de azida de sodio utilizadas, no permitían que la reacción se llevara a cabo por completo y el sodio, uno de los productos obtenidos, reacciona violentamente con el agua.
Los investigadores lograron mejorar las pastillas adicionándoles disulfuro de molibdeno, MoS2, que actúa como lubricante. Sin embargo, esta mezcla no se descompone bien, la adición de azufre, produce pastillas que arden mejor y, con ello, una mejor descomposición y transformación del sodio metálico en sulfato, aunque el residuo sólido era muy fino y difícil de recoger. También se comprobó que, con una mezcla de azida de sodio y óxido de hierro (III) se obtenían residuos sólidos de fácil manipulación.
Después de una serie de ensayos y evaluando los resultados obtenidos, los investigadores propusieron mezclar todos los compuestos que proporcionan a las pastillas las propiedades más adecuadas: azida de sodio, óxido de hierro (III), disulfuro de molibdeno y azufre. Con ello se logró el resultado deseado.
BIBLIOGRAFÍA
1. WHITTEN W., DAVIS R., PECK M., STANLEY


No hay comentarios:
Publicar un comentario